Retiran del mercado pastillas etiquetadas como relajante muscular que contienen medicamentos para la artritis
La empresa Unichem Pharmaceuticals retiró del mercado un lote de un relajante muscular ya que las píldoras del frasco podrían no ser las que figuran en la etiqueta.
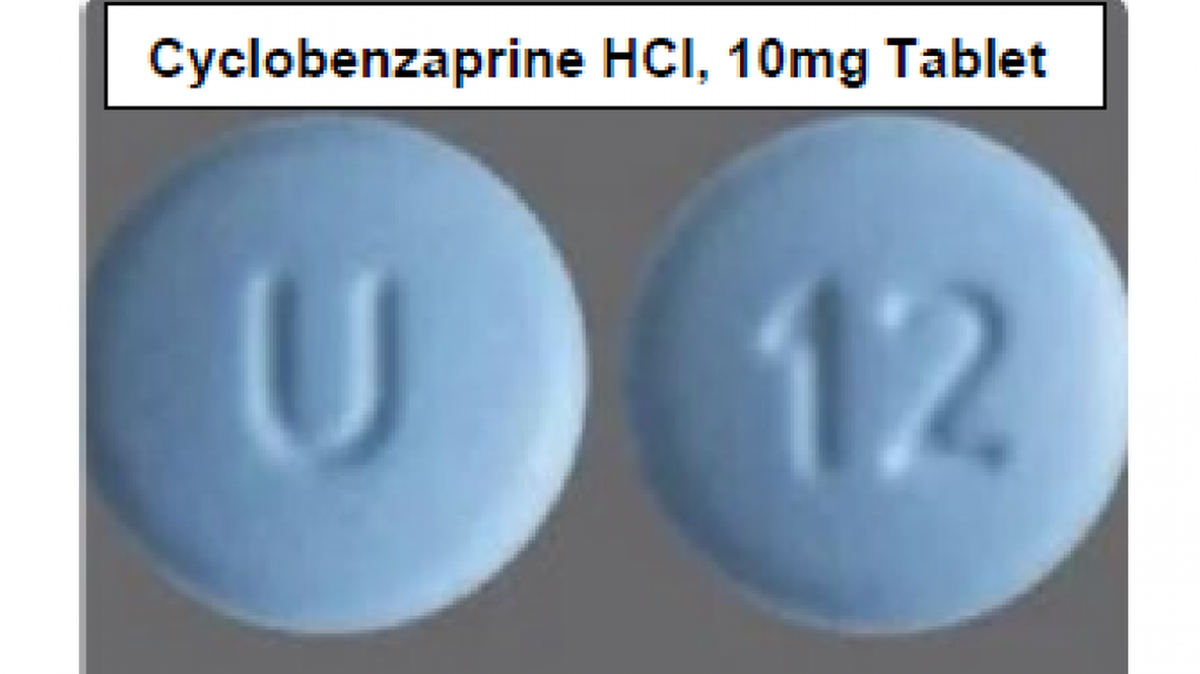
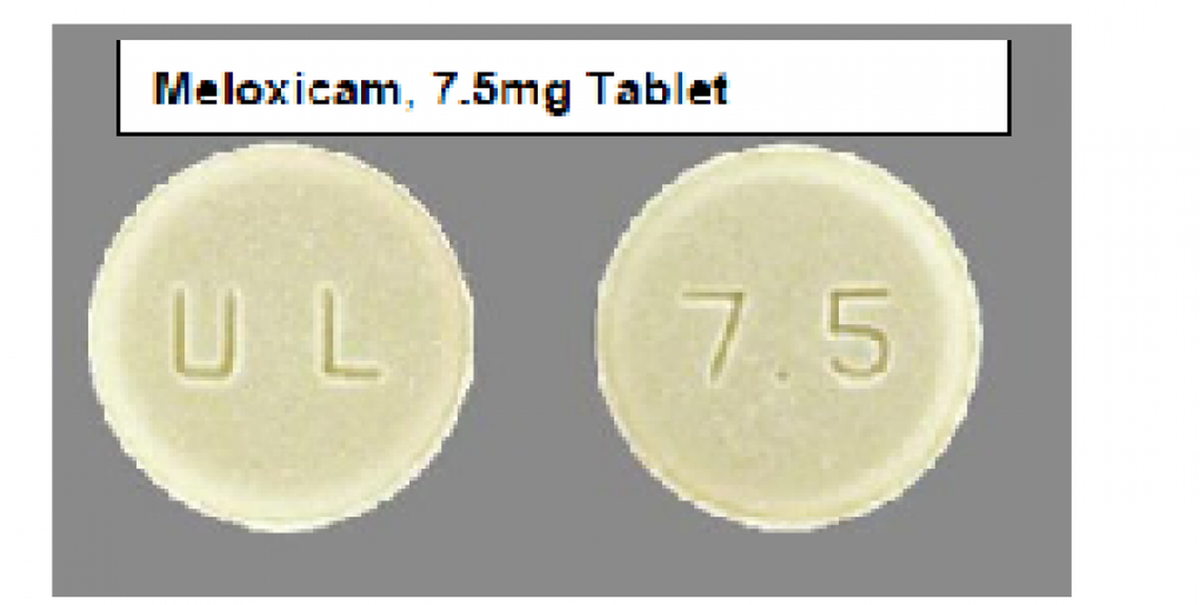
El aviso de retirada de la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) y de la compañía, con sede en East Brunswick, New Jersey, indica que la etiqueta de los frascos de 90 comprimidos de clorhidrato de ciclobenzaprina de 10 mg se colocó en al menos un frasco de comprimidos de meloxicam de 7.5 mg. El meloxicam es un antiinflamatorio no esteroideo que trata diversas formas de artritis.
“Para los pacientes que toman meloxicam sin saberlo, existe una probabilidad razonable de sufrir efectos adversos graves, como reacciones cardiovasculares, gastrointestinales, renales, de anafilaxia y cutáneas”, indica la declaración de riesgo de la retirada.
Esto se aplica sobre todo a aquellas personas que toman anticoagulantes o antiinflamatorios, a personas alérgicas al meloxicam o a personas con una afección médica preexistente.
Las tabletas de ciclobenzaprina son azules con un número “12” en una cara y una “U” en la otra. Las tabletas de meloxicam son amarillas con una “U y L” en una cara y un “7.5” en la otra. El lote que se ordenó recoger tiene el número GMML24026A y su fecha de caducidad es septiembre de 2027.
Si usted es consumidor, devuelva las tabletas retiradas a la farmacia donde las adquirió. Dirija cualquier pregunta que tenga a Inmar, que se está encargando del retiro de Unichem, llamando al teléfono 877-840-5109 o a rxrecalls@inmar.com, de lunes a viernes, de 10:00 a. m. a 6:00 p. m., Hora Estándar del Este. Se le pide a las farmacias que notifiquen a los consumidores y llamen a Inmar para obtener instrucciones sobre cómo devolver las tabletas retiradas.
Consulte a un profesional médico si tiene algún problema de salud. Luego, notifique a la FDA a través del programa MedWatch, ya sea completando el formulario por internet o llamando al 800-332-1088 para obtenerlo y enviándolo luego por correo postal a la dirección que figura en el formulario o por fax al 800-FDA-0178.
Traducción de Jorge Posada
